新型智能载体-活性氧响应型脂质体通过调控肿瘤微环境增强光/化学动力学治疗
肿瘤微环境具有局部乏氧、同时具有较高浓度的还原性物质(如GSH)等特点,并因此限制了多种癌症治疗技术的疗效。在新兴的癌症治疗技术中,化学动力学治疗(CDT)方法主要利用特定价态的金属离子与过氧化氢(H2O2)之间的芬顿反应产生强氧化性羟基自由基,对肿瘤细胞进行杀伤,但由于肿瘤微环境微酸性(pH 6.5~7.0)不足,H2O2供应有限,GSH可能对羟基自由基的产生有抑制等因素,CDT治疗效果受到影响。光动力学治疗(PDT)方法的疗效也会因为肿瘤病灶区域局部乏氧的特点大打折扣。因此,对肿瘤微环境进行调控和改造对高效癌症治疗十分关键,利用肿瘤微环境特征发展肿瘤微环境特异性激活的高效治疗将具有积极意义。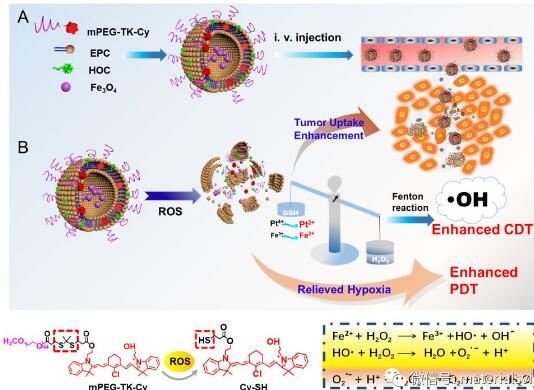
苏州大学功能纳米与软物质研究院刘坚教授和中科院上海药物研究所于海军研究员合作报道了一种可被活性氧(ROS)激活的脂质体(RALP),应用于改造肿瘤微环境,协同增强PDT/CDT治疗癌症的疗效。实验设计的RALP@HOC@Fe3O4包含了对ROS有响应的硫酮键(thioketal bond)的脂质体,当与ROS发生化学反应而剪切断键后,可有效增强药物递送体系在肿瘤细胞的穿透和摄取,并实现响应型的药物释放。共负载Fe3O4纳米颗粒和奥沙利铂前药的RALP能消耗GSH,对肿瘤乏氧微环境进行改造增加了PDT的疗效。当奥沙利铂前药(毒性较低)与肿瘤细胞内的GSH发生反应对其消耗的同时,生成了具有高毒性的奥沙利铂可增加对肿瘤的杀伤。而GSH的消耗既可以避免PDT过程中ROS被过度湮灭,而且也可以调节肿瘤中的化学物种平衡以提高H2O2的产生,有助于和RALP中的Fe (II)发生芬顿反应生成羟基自由基以实现协同增强的CDT。该设计思路创新提出了调控肿瘤微环境进而协同增强PDT/CDT,采用的原料生物相容性好,疗效在细胞和活体动物实验中得到了良好验证,具有临床转化前景
| 温馨提示:苏州贝壳纳米供应产品仅用于科研,不能用于人体,不同批次产品规格性能有差异。网站部分文献案例图片源自互联网,图片仅供参考,请以实物为主,如有侵权请联系我们立即删除。 |
上一篇: 生物仿生结构材料






